Die Animal Welfare Serie
Folge 4
Neuer Therapieansatz für eine genetische Hauterkrankung dank Mäusestudien
Congenital melanocytic naevus syndrome (CMN) ist eine seltene, genetisch bedingte Hauterkrankung, bei der bis zu 80% der Haut mit grossen, juckenden oder sogar schmerzhaften Muttermalen bedeckt ist, die zu Hautkrebs führen können. Anders als die meisten Muttermale, welche sich erst später entwickeln, sind diese sogenannten «Nävi» schon seit Geburt vorhanden. Die bisherigen Behandlungsmöglichkeiten sind begrenzt: Aufwendige Operationen oder Laserbehandlungen können die Muttermale teilweise entfernen, verringern das Krebsrisiko jedoch kaum. Medikamente lindern meist nur die Symptome wie Juckreiz, Schmerzen oder Krampfanfälle.
Dreijährige verhilft zu grossem Fortschritt
Die dreijährige Ada liebt das Meer und darin zu schwimmen, ein unbeschwerter Strandbesuch ist jedoch kaum möglich ohne besonders strenge Vorsichtsmassnahmen. Denn 70% ihrer Haut ist mit CMN bedeckt. Diese lösen bei ihr oft Juckreiz und Schmerzen aus. Im Rahmen eines Forschungsprojekts für neue Behandlungsmöglichkeiten spendete sie dem Francis-Crick-Institut in London Hautzellen.
Die Forschenden nutzten die Zellen, um ein innovatives Behandlungsverfahren zu testen: Ziel war es, das mutierte NRAS-Gen zu deaktivieren – jenes Gen, das die krankhaften Muttermale auslöst. In ersten Versuchen in der Petrischale gelang es, die Genaktivität gezielt zu unterdrücken.
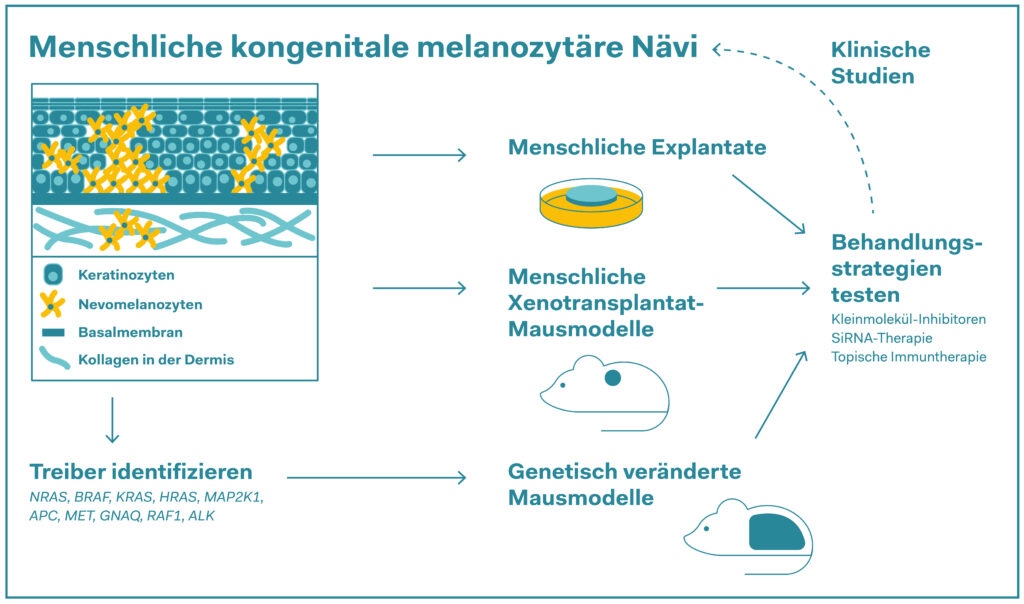
Präklinische Forschungsstrategien zur Erprobung neu entwickelter Therapien für kongenitale melanozytäre Nävi (CMN). Die bekannten Ursachen von CMN, einschliesslich der Gene mit definierten Mutationen oder Fusionen, sind aufgelistet, und alle vorgeschlagenen Behandlungsstrategien sind in dem Schema enthalten.
Quelle: Emerging Therapies for Congenital Melanocytic Nevi, 2025
Tests an Mäusen schüren Hoffnung
Im nächsten Schritt wurde die potenzielle Therapie in einem Tierversuch getestet – ein unverzichtbarer Schritt, um Wirkung und Sicherheit im lebenden Organismus zu prüfen. Die Forschenden injizierten Mäusen mit CMN das neue Medikament. Bereits nach 48 Stunden zeigte sich eine Wirkung: Das mutierte Gen wurde unterdrückt, die krankhaften Hautveränderungen begannen sich zurückzubilden.
Dr. Veronica Kinsler, leitende Ärztin und Wissenschaftlerin am Crick-Institut und Mitglied des Forschungsprojekts, zeigt sich erfreut. Die Tatsache, dass die Muttermale verschwinden sowie die erfolgreiche Verabreichung an Mäuse, seien Meilensteine in der CMN-Forschung und lösen Hoffnung für Betroffene und Angehörige aus. Zwar müssen noch weitere Tests durchgeführt werden, bevor die Therapie an Menschen geprüft werden kann. Die Mäusestudie aber war ein nötiger Schritt, um wichtige Erkenntnisse über die Wirkung und Risiken der Therapie zu erlangen.
Neue Hoffnung für Betroffene – und die Forschung
Auch Eltern äusserten sich zu den Resultaten. Die Aussicht, dass die Krankheit ihrer Tochter zukünftig geheilt und so das Hautkrebsrisiko ihrer Tochter erheblich vermindert werden könne, habe ihre Erwartungen gesprengt. «Der Gedanke, dass diese Therapie in nur wenigen Jahren erhältlich sein könnte, ist überwältigend.»
Nebst dem therapeutischen Fortschritt zeigt das Projekt auch die Stärke moderner Forschung: Durch die Kombination von Zellmodellen im Labor und Tierversuchen können neue Behandlungen heute gezielter, schneller und sicherer entwickelt werden. Die Studie unterstreicht, wie wichtig Tierversuche trotz der Fortschritte in alternativen Methoden weiterhin sind, um den letzten entscheidenden Schritt zur sicheren Anwendung am Menschen zu gehen.
Weiterführende Informationen:
- Researchers find potential of mole reversal therapy in rare condition. News an features; The Francis Crick Institute, 17 June 2024
- RNA Therapy for Oncogenic NRAS-Driven Nevi Induces Apoptosis. Journal of Investigative Dermatology, Volum 145, Issue 1, P122-134, January 2025.
- Emerging Therapies for Congenital Melanocytic Nevi: Journal of Experimental Pathology, 2025 ;6 (1).
Tierversuche sind in der biomedizinischen Forschung oft unerlässlich, um die Sicherheit und Wirksamkeit neuer Therapien zu beurteilen. Sie bieten Einblicke in die komplexen Wechselwirkungen innerhalb eines lebenden Organismus, die in Alternativmethoden allein nicht erfasst werden können. Die Forschung entwickelt zunehmend alternative Methoden wie Organoide, um den Einsatz von Tieren immer weiter zu reduzieren.